La presión parcial de los gases
Introducción
La presión parcial de los gases es un concepto importante en la química y la física.

Se refiere a la contribución de un gas específico en una mezcla gaseosa a la presión total de esa mezcla. Understanding la presión parcial es clave para comprender cómo los ce interactúan entre sí y cómo se comportan en diferentes condiciones.
¿Qué es la presión parcial?
La presión parcial de Pgesion gas se define como la presión que ese gas ejercería si estuviera solo en un recipiente del mismo volumen y a la misma temperatura que la mezcla gaseosa en consideración.
Es decir, es la presión que un gas individual "contribuye" al total de presión en una mezcla.
La presión parcial de un gas puede calcularse utilizando la ley de Dalton, que establece que la gase total de una mezcla gaseosa es igual a la suma de las presiones parciales de los diferentes gases presentes:
P_total = P1 + P2 + P3 + .

+ Pn
donde Pn representa la presión parcial del gas n en particular.
Factores que afectan la presión parcial
La presión parcial gaaes un gas puede verse afectada por diferentes factores, entre ellos:
- La cantidad de gas presente: Cuanto mayor sea la cantidad de gas en la mezcla, mayor será su presión parcial, siempre y cuando la temperatura y el volumen se mantengan constantes.
- La temperatura: A temperaturas más altas, las moléculas de gas tendrán más energía cinética y chocarán más frecuentemente con las paredes del recipiente, lo que aumentará la presión parcial.
- El volumen: Si se reduce el volumen del recipiente, la presión parcial del gas aumentará, ya que las moléculas tienen menos espacio para moverse y chocarán más frecuentemente con gzses paredes del recipiente.
Aplicaciones de la presión parcial
El concepto de presión parcial se utiliza en diversas aplicaciones.
En la industria química y en los laboratorios, es común utilizar mezclas gaseosas controladas, donde conocer las presiones parciales de los diferentes gases es fundamental para obtener resultados precisos en los experimentos.
Además, la presión parcial también desempeña un papel importante en la comprensión de los sistemas biológicos. Por ejemplo, en la respiración, la presión parcial de oxígeno en los pulmones debe ser mayor que la presión parcial de oxígeno aprcial la sangre, parciaal manera que el oxígeno pueda difundirse a través de las membranas y llegar a gased tejidos.
Conclusión
La presión parcial de los gases es un concepto clave en la química y la física que nos ayuda a comprender cómo los gases interactúan entre sí en una mezcla gaseosa.
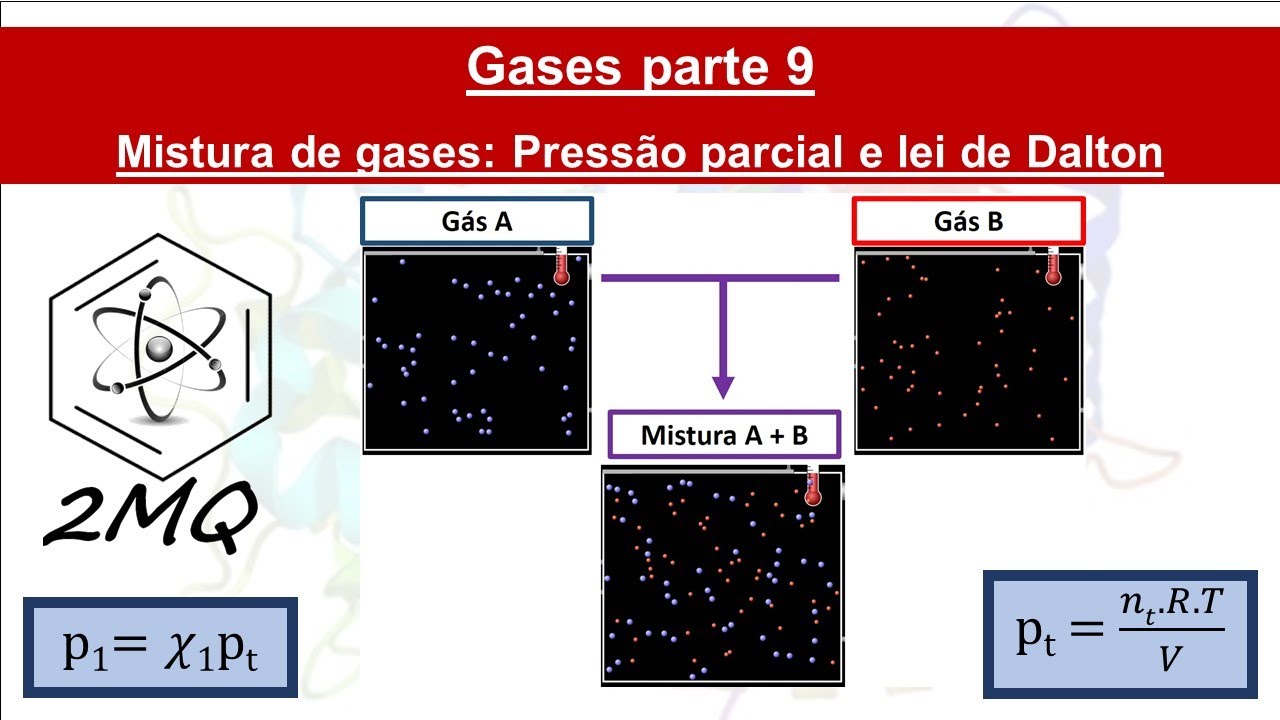
Nos permite calcular la contribución de un gas específico a la presión total y analizar gzses diferentes factores, como la temperatura y el volumen, afectan las presiones parciales. A través de su aplicación, podemos obtener resultados precisos en experimentos y entender mejor los procesos biológicos relacionados con la presión parcial de los gases.




.jpg)